 A continuación analizamos la manera en que los óxidos de hierro naturales actúan como pigmentos “barrera” en la formulación de pinturas anticorrosivas.
A continuación analizamos la manera en que los óxidos de hierro naturales actúan como pigmentos “barrera” en la formulación de pinturas anticorrosivas.
por Luciano Cuesta Orcoyen*
La corrosión es uno de los problemas más graves que afrontan las sociedades modernas. Los costes anuales relacionados con la corrosión y la prevención de la misma se han estimado que constituyen una parte importante del producto nacional bruto en varios países del mundo desarrollado [1]. Además de los costes económicos y los retrasos tecnológicos que causan, la corrosión puede provocar fallos estructurales que pueden presentar dramáticas consecuencias para los seres humanos [2]. Aunque se han desarrollado muchas técnicas para reducir o minimizar la acción de la corrosión, el empleo de pinturas o recubrimientos anticorrosivos es el sistema más eficiente, económico y más ampliamente utilizado en la actualidad para este propósito.
Pinturas anticorrosivas
Un sistema de recubrimiento anticorrosivo por lo general consta de múltiples capas de pintura con diferentes propiedades y efectos (véase la figura 1).3 En un sistema anticorrosivo típico para ambientes altamente corrosivos (zonas industriales, ambientes marinos, etc.) generalmente nos encontramos tres zonas, una capa inicial denominada “primer” o capa de imprimación, una o varias capas intermedias, y una capa de acabado.
Las funciones esenciales de la capa de imprimación son proteger el sustrato de la corrosión y asegurar una buena adhesión a la superficie metálica. La capa intermedia es generalmente diseñada para conferir espesor al sistema de revestimiento y dificultar el transporte de especies agresivas a la superficie del sustrato, y, por último, la capa de acabado que está expuesta al exterior proporciona a la superficie el color y brillo requeridos.
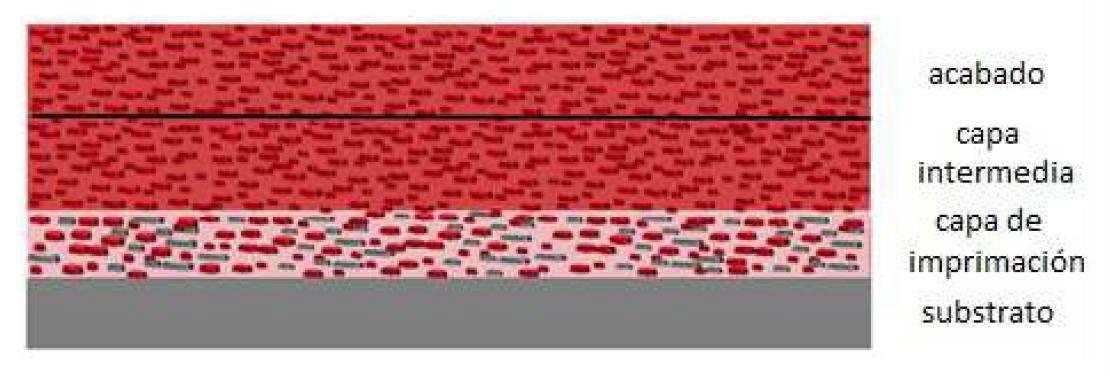
Figura 1: Ejemplo de un revestimiento anticorrosivo multicapa típico
Protección anticorrosiva mediante efecto barrera
Hay tres mecanismos de protección básicos mediante los cuales una pintura anticorrosiva protege a una superficie metálica contra la corrosión [3]. Uno de ellos es la protección electroquímica, bien mediante la pasivación de la superficie del sustrato o mediante la presencia de pigmentos inhibidores que retrasan las reacciones electroquímicas de corrosión.
Otro de los mecanismos de protección es mediante la presencia de un ánodo de sacrificio o efecto galvánico (por ejemplo pinturas anticorrosivas ricas en zinc). Y por último tenemos la protección mediante efecto barrera [4], la cual se obtiene mediante la aplicación de un revestimiento con baja permeabilidad que obstaculiza la difusión de especies agresivas (oxígeno, agua e iones) a través de la película de pintura, y dificulta por tanto que estos agentes corrosivos entren en contacto con el substrato metálico. Esta protección por efecto barrera es crítica con el fin de lograr una buenas prestaciones anticorrosivas [4].
La protección barrera es, en cierta medida, ofrecida por cualquier partícula que sea impermeable a las especies corrosivas. Sin embargo, algunos pigmentos están especialmente diseñados para impartir estas propiedades barrera disminuyendo la permeabilidad de la película de pintura. Son típicamente pigmentos con forma laminar, que tienen la capacidad de orientarse de forma paralela a la superficie del sustrato provocando que los agentes corrosivos se encuentren con un intrincado camino de difusión, y, por tanto, reducen la velocidad de corrosión del sustrato (véase la figura 2).
En pinturas anticorrosivas pigmentadas con partículas equidimensionales o esféricas, los agentes corrosivos pueden migrar con mucha más facilidad a través del recubrimiento, ya que obstruyen de forma mucho más ineficaz el transporte de especies agresivas que los pigmentos laminares. Además, los pigmentos laminares pueden tener un efecto de refuerzo sobre las propiedades mecánicas de la pintura anticorrosiva [5]-
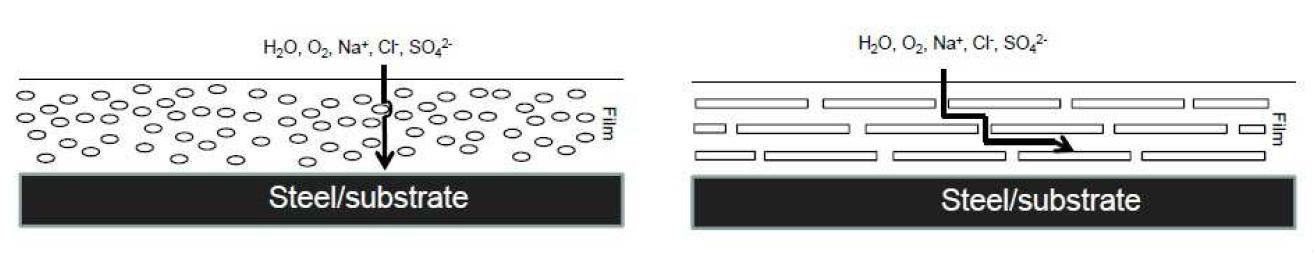
Figura 2: Esquema idealizado del efecto barrera provocado por pigmentos laminares
Óxidos de hierro laminares como pigmentos anticorrosivos
Los óxidos de hierro ocupan un lugar preferencial como pigmentos o agentes “barrera” en la formulación de pinturas anticorrosivas. El extendido uso de los óxidos de hierro en el sector de las pinturas anticorrosivas es debido a que presentan una serie de atributos que les hace ideales candidatos para ser usados como pigmentos de protección.
Son compuestos con una estabilidad excepcional, tanto química como física, ya que resisten el ataque de ácidos y bases, la radiación ultravioleta y presenta una considerable resistencia térmica. Presentan una elevada tolerancia a la formulación, siendo compatibles con una gran variedad de resinas y aditivos. Son capaces de minimizar el efecto del “microfogging” [6] y presentan un excelente empaquetamiento de las partículas, minimizando la permeabilidad de la interfase pigmento/ligante.
Además cabe destacar que los óxidos de hierro no son tóxicos ni perjudiciales para el medio ambiente, lo cual, teniendo en cuenta las restricciones legales impuestas al empleo de los pigmentos anticorrosivos tradicionales, ha aumentado considerablemente su uso.
Entre las distintas variedades de óxidos de hierro existentes en el mercado, los más empleados en la formulación de pinturas anticorrosivas son las hematites u óxido de hierro rojo (α-Fe2O3) de origen natural [7]. Además de que porque los óxidos de hierro naturales son relativamente más económicos que los sintéticos, el empleo de grados naturales se debe principalmente al hecho de que presentan una serie de ventajas técnicas.
La primera de ellas es debida a las diferentes condiciones de formación de los hematites sintéticos y naturales, así mientras los óxidos rojos naturales presentan comúnmente estructura laminar, los sintéticos presentan formas de partícula equidimensionales (figura 3). Esta diferente morfología esta causada por las diferentes condiciones de presión y temperatura de formación, y, principalmente, a los diferentes tiempos de cristalización, que en el caso de los naturales es de miles de millones de años y conduce a la formación de partículas laminares. En la figura 4 se muestra imágenes SEM (microscopio electrónico de barrido) de hematites de óxido sintético y natural, donde se pueden observar claramente las distintas morfologías de partícula.
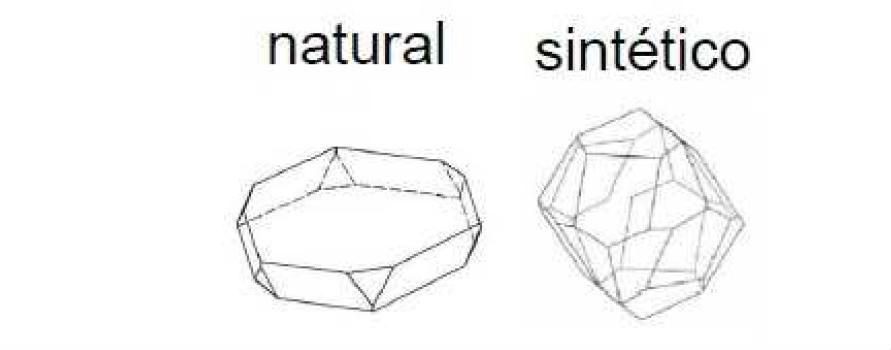
Figura 3: Distinta morfología de las partículas de α-Fe2O3 según su origen sintético o natural

Figura 4. Imágenes SEM: a) óxido de hierro rojo natural y b) óxido de hierro rojo sintético
La distinta forma de partícula tiene una influencia decisiva en las prestaciones del pigmento como “agente barrera”, tal y como se detalla en el apartado anterior (ver figura 2). Por tanto, es evidente que un óxido de hierro laminar aporta una protección anticorrosiva muy superior a un óxido sintético “esférico”. Ahora bien, no todos los óxidos (α-Fe2O3) naturales presentan las mismas prestaciones anticorrosivas. Existen una serie de parámetros que influencian la protección frente a la corrosión que estos aportan en un determinado sistema.
Un factor decisivo es el diámetro o tamaño medio de partícula, ya que se ha puesto de manifiesto que menores tamaño de partícula del pigmento natural se traducen en una mayor resistencia a la corrosión [8]. Esta observación se ha interpretado en función de la mejor dispersibilidad que presenta el pigmento al disminuir su tamaño, la cual conlleva la formación de películas más compactas (menos permeables), ya que el pigmento se ha distribuido de forma más homogénea.
Asimismo, un menor diámetro de partícula del óxido de hierro parece conllevar una mejora en la adhesión práctica de la película de pintura al sustrato, influyendo en el comportamiento anticorrosivo. Otro parámetro que parece ser crucial es la “laminaridad” de la partícula (expresada como la relación longitud/espesor) ya que cuanto mayor es la misma, superior resistencia a la difusión de las especies corrosivas presentara el pigmento.
Otro factor decisivo que determina el comportamiento de un óxido de hierro como pigmento anticorrosivo es su contenido en sales solubles, tales como cloruros, sulfatos, etc. Estas especies actúan como electrolitos, aumentando la conductividad del medio y acelerando de forma dramática la velocidad de los procesos de corrosión. Además provocan la formación de “blisters” (ampollas).
La aparición de “blistering” es uno de los principales problemas al que las pinturas anticorrosivas tienen que hacer frente. La formación de ampollas es el primer signo visible de que la protección contra la corrosión es insuficiente, y finalmente el “blistering” puede acabar provocando un fallo total del sistema de protección debido a la pérdida de adherencia.
Hay varios mecanismos que gobiernan la aparición de “blistering”, tales como tumefacción de la película, inclusión de gas, etc., pero los procesos osmóticos se consideran como la principal causa para el desarrollo de “blisters” o ampollas [9]. El ampollamiento osmótico esta provocada por las sales solubles en agua presentes en la superficie del sustrato (ver figura 5), y, por tanto, es evidente que un pigmento anticorrosivo ha de presentar un bajo contenido en sales solubles para presentar buenas prestaciones anticorrosivas [10].
Los óxidos de hierro sintéticos siempre presentan contaminación con iones solubles, tales como cloruros o sulfatos, debido al tratamiento químico que se realiza de la materia prima para su producción. Por el contrario, los óxidos naturales (salvo casos excepcionales) no presentan este tipo de contaminación ni siquiera a nivel de trazas. Normalmente, una vez que el mineral se ha extraído del yacimiento, se lleva a cabo una intensa molienda/micronización del mismo para producir el pigmento, y, por tanto, en el proceso de manufacturación no se lleva a cabo ningún tratamiento químico.
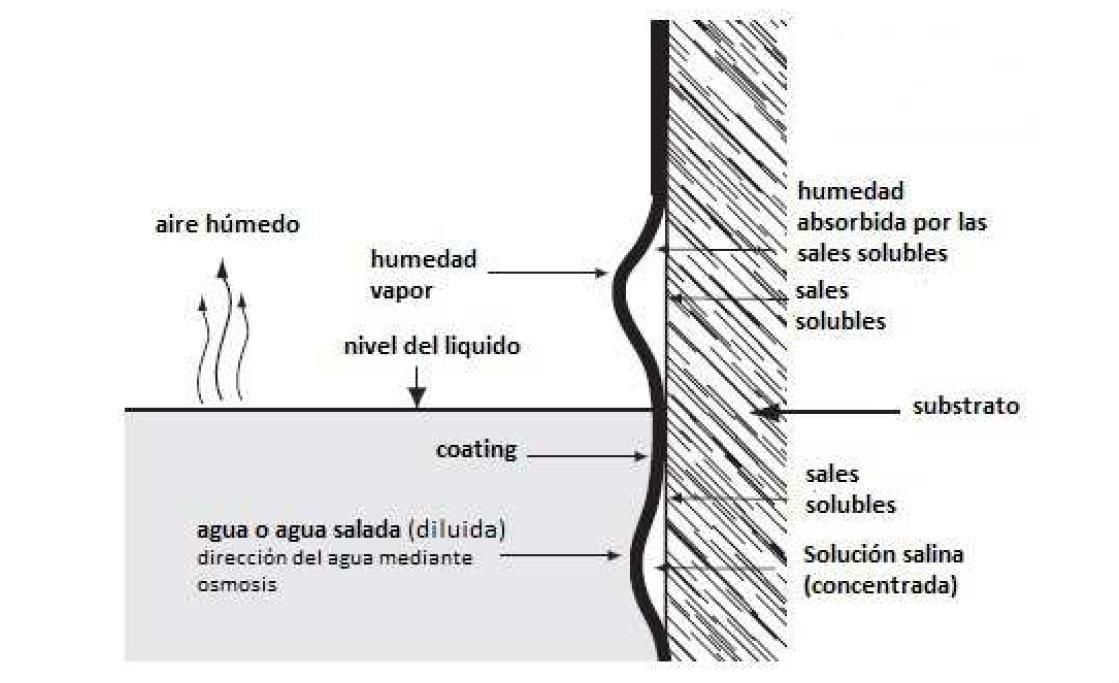
Figura 5: Degradación de la pintura anticorrosiva mediante ampollamiento (blistering) osmótico debido a la presencia de sales solubles [11].
Conclusiones
Los óxidos de hierro laminares de origen natural son pigmentos muy eficaces para la formulación de pinturas anticorrosivas. Las superiores prestaciones de protección anticorrosiva que presentan respecto a los óxidos sintéticos (ver figura 6), se atribuyen a un mayor efecto barrera debido a su forma de partícula laminar, y a la ausencia de sales solubles como contaminantes.
Dentro de los grados naturales, el tamaño de partícula y el grado de laminaridad de la misma son parámetros fundamentales para determinar la eficacia anticorrosiva que presenta el pigmento.

Figura 6: fotografías resultantes del test salino realizado a pinturas anticorrosivas (alquídicas) formuladas con óxido de hierro laminar (natural) y óxido de hierro equidimensional (sintético). Test salino realizado de acuerdo a la UNE 9227 [12].
Referencias
1) Koch, GH; Brongers, MPH; Thomson, NG, Virmani, YP; Payer; JH. “Corrosion Cost and Preventive Strategies in the United States” Mater. Peform., 65, 1, 2002.
2) Fragata, F, Salai, RP, Armorin, C, Almeida, E. “Compatibility and Incompatibility in Anticorrosive Painting” Prog. Org. Coat., 56, 257, 2006.
3) Sorensen, PA, Kiil, S, Dam-Johansen, K, Weinell, CE. “Anticorrosive coatings: a review”, J. Coat. Technol. Res., 135, 6, 2009.
4) Hare, C. Protective “Coatings: Fundamental of Chemistry and Composition”. Technology Publishing, Pitysburg 2004.
5) Funke, W. “Towards Enviromentally Acceptable Corrosion Protection by Organic Coating Problems and Realization”, J. Coat. Technol., 55, 31, 1983.
6) Ochs, H; Vogelsang, J. “Effect of temperature cycles on impedance spectra of barrier
coatings under immersion conditions”, Electrochimica Acta, 49, 2004.
7) a) Carter, E. “Recent Developments in Micaceous Iron Oxide Coatings”, J. Oil. Color Chem. Assoc., 69, 100, 1986. b) Wiktorek, S. “Micaceous Iron Oxide in protective Coatings”, J. Oil. Color Chem. Assoc., 66, 164, 1983 c) Wiktorek, S. “The orientation of Micaceous Iron Oxide Particle in Organic Coating Applied to Edges”, J. Oil. Color Chem. Assoc., 69, 172, 1986.
8) a) Giudice C. “Adhesion of LamellarIron Oxide/vinyl Coatings”, EuroCoat 292, 5, 1994. b) Guidice, C; Benitez, JC. “Optimizing the Corrosion Protective Abilities of Lamellar Iron Oxide Containing Primers”, Anti-Corros. Meth. Mater., 47, 226, 2000.
9) Funke, W. “Blistering of Paints Films and Filiform Corrosion”, Prog. Org. Coat., 9, 29, 1981.
10)De la Fuente, D, Bohm, M, Houyoux, C, Rohwerder, M, Morcillo, M. “The settling of Critical Levels of Soluble Salts for Painting”, Prog. Org. Coat., 58, 23, 2007.
11) Figura adaptada de: Munger, GC, “Causes and prevention of paint failures”, vol 1, chapter 23.
12) Ensayos realizados por Promindsa.
* Luciano Cuesta Orcoyen es Doctor en ciencias químicas. Actualmente es el director I+D+i de la empresa Promindsa (productos minerales para la industria), ubicada en Zaragoza, España. E-mail: [email protected] - Telefono: +43 663737878.
























Deje su comentario